Pelarut
Pelarut atau solvent merupakan bagian penting dalam pelarutan. Jenisnya dapat dibedakan menjadi beberapa golongan atau kategori tergantung sifat kimia dan wujudnya. Kategori berdasar sifat kimia yaitu polar dan non polar serta organik dan anorganik, sedangkan berdasarkan wujudnya berupa cair, padat, dan gas. Contoh solvent polar misalnya air, etanol dan metanol. Solvent semipolar misalnya etil asetat dan diklormethan, sedangkan solvent nonpolar n-heksan, petroleum eter, dan kloroform.

Lestari dkk., (2025) mengemukakan bahwa solvent digunakan untuk pemisahan antar komponen dengan distilasi, ekstraksi, dan kromatografi. Menurut Hujjatusnaini (2021), solvent sangat umum digunakan untuk ekstraksi, yaitu pemisahan komponen dari campurannya dengan solvent sebagai pemisah. Pada umumnya jumlah zat yang terlarut (solut) lebih sedikit dibandingkan jumlah solvent. Larutan dengan jumlah maksimum zat terlarut pada temperatur tertentu disebut larutan jenuh. Sebelum mencapai titik jenuh disebut larutan tidak jenuh. Sedangkan jika zat terlarut melebihi jumlah solvent disebut larutan lewat jenuh.
Konsentrasi Larutan
Komposisi zat terlarut dengan solvent disebut dengan konsentrasi larutan yang dinyatakan dalam satuan fisik. Satuan ini meliputi satuan berat atau satuan volume dan satuan kimia, misalnya mol, massa rumus, dan ekuivalen.
a. Persen Konsentrasi
Dalam bidang kimia sering digunakan % untuk menyatakan konsentrasi larutan. Persen konsentrasi dapat dinyatakan dengan persen berat (%W/W) dan persen volume (%V/V)

b. Parts per Million (ppm) dan parts per billion (ppb)
Bila larutan sangat encer digunakan ppm (bagian per juta) dan ppb (bagian per miliar). 1 ppm ekuivalen dengan 1 mg cat terlarut dalam 1 L larutan. Sedangkan 1 ppb ekuivalen dengan 1 miu gram zat terlarut per 1 L larutan.

Ppm dan ppb merupakan satuan yang mirip dengan persen berat. Bila persen berat, gram zat terlarut per 100 g larutan, maka ppm gram terlarut per sejuta gram larutan, dan ppb zat terlarut per miliar gram larutan.

c. Fraksi mol

d. Molaritas/kemolaran (M)
Molaritas atau konsentrasi molar (M) suatu larutan jumlah mol spesi zat terlarut dalam 1 liter larutan atau jumlah milimol dalam 1 ml larutan.
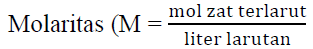
e. Molalitas/kemolalan (m)
Kemolalan (m) menyatakan jumlah mol zat terlarut dalam 1000 g pelarut. Kemolalan tidak tergantung pada temperatur dan digunakan dalam bidang kimia fisika, teristimewa dalam sifat koligatif.
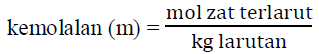
f. Normalitas/kenormalan (N)

